Warto zakupić generator podchlorynu sodu. Koszt jest bardzo niewielki.
Niewiela ilość soli niejodowanej oraz przykładowy generator zapewni nam wystarczającą ilość podchlorynu sodu w dowolnym miejscu i czasie.
Doświadczenie w użyciu tego konkretnego urządzenia podpowiada, że należy proces wykonać najlepiej dwukrotnie, a nie jak jest w instrukcji jeden raz.
Główną funkcją generatora podchlorynu sodu (NaClO) jest produkcja roztworu podchlorynu sodu na miejscu (in situ) poprzez elektrolizę wodnego roztworu soli kuchennej (NaCl).
Warto dokupić do niego Tester PH.

Podchloryn sodu (NaClO) ma zasadowe pH, które zależy od jego stężenia. W typowych zastosowaniach jego pH mieści się w zakresie 11–13.
📊 Przykładowe wartości pH w zależności od stężenia:
| Stężenie NaClO | pH roztworu |
|---|---|
| 0,1% | ok. 10,5–11 |
| 1–5% (np. woda basenowa) | ok. 11–12,5 |
| 10–15% (techniczne, przemysłowe) | 12–13,5 |
🔬 Dlaczego NaClO ma wysokie pH?
Podchloryn sodu w wodzie ulega częściowemu rozpadowi do: NaClO+H2O⇌NaOH+HClONaClO + H_2O ⇌ NaOH + HClO
- NaOH (wodorotlenek sodu) jest silną zasadą → powoduje wzrost pH.
- Im wyższe stężenie NaClO, tym więcej NaOH w roztworze.
🧪 Znaczenie pH w praktyce:
- Wysokie pH sprawia, że NaClO działa lepiej jako środek dezynfekujący, ale:
- przy pH > 11 przeważa forma podchlorynu (ClO⁻), która jest mniej skuteczna niż kwas podchlorawy (HClO).
- Dlatego w niektórych zastosowaniach (np. w uzdatnianiu wody) pH obniża się do 6–7, aby zwiększyć zawartość aktywnego HClO.
Podsumowanie:
- Typowe pH podchlorynu sodu: 11–13
- Im wyższe stężenie, tym wyższe pH
- W praktyce często reguluje się pH, by zoptymalizować działanie dezynfekcyjne
⚙️ Jak działa generator podchlorynu sodu?
Generator wykorzystuje proces elektrolizy, w którym:
- przez roztwór soli (NaCl) przepuszczany jest prąd elektryczny,
- na anodzie i katodzie zachodzą reakcje chemiczne,
- w wyniku tego powstaje:
➤ podchloryn sodu (NaClO) – główny produkt,
➤ gazowy chlor (Cl₂) – w małych ilościach,
➤ wodorotlenek sodu (NaOH) i wodór (H₂).
🧪 Reakcja (uproszczona):
NaCl+H2O→elektrolizaNaClO+H2NaCl + H_2O \xrightarrow{elektroliza} NaClO + H_2
🧼 Zastosowania podchlorynu sodu z generatora:
- Dezynfekcja wody pitnej
- w stacjach uzdatniania wody,
- w oczyszczalniach ścieków.
- Dezynfekcja wody basenowej
- Przemysł spożywczy
- dezynfekcja instalacji (CIP),
- mycie warzyw i owoców.
- Zastosowania medyczne i sanitarne
- Rolnictwo
- dezynfekcja systemów nawadniania i powierzchni.
✅ Zalety stosowania generatora:
- Brak konieczności magazynowania gotowego, niestabilnego chemicznie NaClO.
- Bezpieczeństwo – unika się transportu i przechowywania toksycznych chemikaliów.
- Ekonomia – sól i prąd są tanie.
- Świeży roztwór – większa skuteczność dezynfekcyjna.
Podsumowanie:
Generator podchlorynu sodu to urządzenie służące do produkcji świeżego roztworu NaClO, głównie do dezynfekcji wody i powierzchni, z wykorzystaniem soli i energii elektrycznej. Jest to ekologiczna i bezpieczniejsza alternatywa dla gotowych środków chemicznych.
Podchloryn sodu (NaOCl) to związek chemiczny stosowany jako środek dezynfekujący, wybielający i oczyszczający wodę. Można go uzyskać na kilka sposobów:
1. Elektroliza wodnego roztworu chlorku sodu (NaCl) – metoda przemysłowa
Reakcja chemiczna: 2NaCl+H2O→NaOCl+H2+NaCl2NaCl + H_2O \rightarrow NaOCl + H_2 + NaCl
Opis:
- Do wody dodaje się sól kuchenną (NaCl) i poddaje elektrolizie.
- Na katodzie wydziela się wodór (H₂), a na anodzie powstaje chlor gazowy (Cl₂).
- Chlor reaguje z wodorotlenkiem sodu (NaOH) tworząc podchloryn sodu (NaOCl).
- Jest to główna metoda produkcji stosowana w przemyśle.
2. Reakcja chloru z wodorotlenkiem sodu – metoda laboratoryjna i przemysłowa
Reakcja chemiczna: Cl2+2NaOH→NaCl+NaOCl+H2OCl_2 + 2NaOH \rightarrow NaCl + NaOCl + H_2O
Opis:
- W tej metodzie gazowy chlor (Cl₂) przepuszcza się przez zimny i rozcieńczony roztwór wodorotlenku sodu (NaOH).
- Powstaje mieszanina chlorku sodu (NaCl) i podchlorynu sodu (NaOCl).
- Metoda ta pozwala na produkcję wybielaczy i środków dezynfekujących.
3. Reakcja dwutlenku manganu z podchlorynem wapnia
Reakcja chemiczna: Ca(OCl)2+MnO2+2NaOH→NaOCl+Ca(OH)2+MnO2Ca(OCl)_2 + MnO_2 + 2NaOH \rightarrow NaOCl + Ca(OH)_2 + MnO_2
Opis:
- Podchloryn sodu można uzyskać z podchlorynu wapnia (stosowanego np. w dezynfekcji wody basenowej) przez reakcję z wodorotlenkiem sodu i tlenkiem manganu(IV).
- Jest to bardziej skomplikowana metoda, ale użyteczna w laboratoriach.
4. Reakcja chloru z węglanem sodu (metoda alternatywna)
Reakcja chemiczna: Cl2+Na2CO3+H2O→NaOCl+NaCl+CO2Cl_2 + Na_2CO_3 + H_2O \rightarrow NaOCl + NaCl + CO_2
Opis:
- Chlor reaguje z węglanem sodu (sodą kalcynowaną) w obecności wody.
- Produktem ubocznym jest dwutlenek węgla (CO₂).
- Metoda ta jest mniej wydajna niż reakcja z NaOH.
Podsumowanie – Najlepsze metody w praktyce
- Elektroliza solanki – najczęściej stosowana w przemyśle.
- Reakcja chloru z NaOH – prosta metoda laboratoryjna i przemysłowa.
- Reakcja podchlorynu wapnia z NaOH – dobra alternatywa.
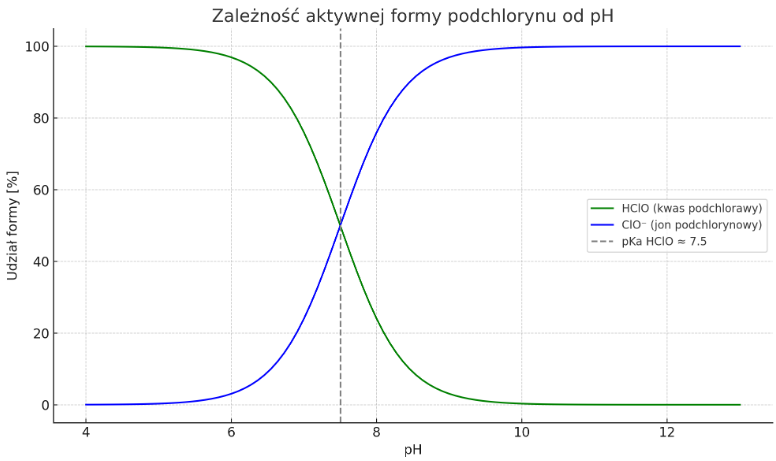
Powyższy wykres pokazuje, jak zmienia się udział aktywnych form podchlorynu sodu w zależności od pH:
- Zielona linia – HClO (kwas podchlorawy): to forma bardziej aktywna biobójczo.
- Niebieska linia – ClO⁻ (jon podchlorynowy): mniej aktywna, ale bardziej stabilna.
🔍 Kluczowe obserwacje:
- Przy pH ~5–7 dominuje HClO → maksymalna skuteczność dezynfekcji.
- Przy pH powyżej 8 rośnie udział ClO⁻, a skuteczność dezynfekcyjna spada.
- W typowych roztworach technicznych NaClO (pH 11–13) dominującą formą jest ClO⁻.
👉 Wnioski praktyczne:
- W uzdatnianiu wody pitnej i basenowej często reguluje się pH (do ok. 6,5–7,5), aby zwiększyć zawartość aktywnego HClO i poprawić efektywność dezynfekcji.

